 BTC/HKD-4.33%
BTC/HKD-4.33% ETH/HKD-4.75%
ETH/HKD-4.75% LTC/HKD-3.96%
LTC/HKD-3.96% ADA/HKD-6.8%
ADA/HKD-6.8% SOL/HKD-8.88%
SOL/HKD-8.88% XRP/HKD-5.83%
XRP/HKD-5.83%界面新聞記者|李科文
界面新聞編輯|謝欣
1
就如《獵藥師:發現新藥的人》一書中直言,新藥研發就像阿根廷作家博爾赫斯的《巴別塔圖書館》中尋找真理的過程一樣困難。被尋找、挑選或設計的,能與人體異常復雜的分子系統配對的某個化合物,就如真理一樣,潛藏在這座像宇宙一般浩瀚無垠的巴別塔圖書館之中。
某種化合物可能消滅卵巢癌細胞,另一種可能會抑制老年癡呆癥的惡化,還有一種或許可以清除艾滋病,但也有可能根本沒有這些能適配的化合物,也就是說真理或許根本就不存在。
現代藥物研發流程卻有著基礎輪廓,是科學家們基于基因學、蛋白組學等生物學研究找到新靶點,然后建立篩選方法,從類藥化合物庫中找到有活性有潛力的苗頭化合物,進一步篩選、優化出為先導化合物,然后再以先導物為基礎通過一系列安全性、活性、成藥性的研究和驗證,發展出藥效、選擇性、其他成藥性質都符合標準的臨床前候選化合物,最后再在幾個候選化合物中持續驗證和探索,直到鎖定一個各方面表現最優、可以進入臨床試驗的候選藥物分子。
目前,人類仍沒有辦法獲取關于人體和化合物全面且確切的信息,就好似未是知的未知。而當代藥物研發人員尋找新藥的困難程度便與在巴別塔圖書館中的圖書管理員相似——大部分圖書管理員在圖書館中窮盡一生也一無所獲,看到的只是雜亂無章的字母,而非真理。
時間的齒輪徑直地轉到2020年。在這一年,Google旗下DeepMind的AlphaFold發布取得重大突破,解決了困擾科學家50年的生物學難題——蛋白折疊。雖然早在1966年,賽勒斯·利文索爾已將計算機模擬與分子圖像相結合實現蛋白質和核酸結構可視化,正式標志著計算機輔助藥物設計的開始,但AlphaFold的驚艷表現讓資本市場對AI在制藥領域對作為用著火熱的期許——這一技術可以幫助科學家看清靶點的結構,新藥研發的第一步從霧里看花轉為按圖索驥,讓很多已知靶點具備了開發成藥的條件,顯著打開創新藥研發源頭的閥門。尋找真理是否能一步到位,有捷徑可循?
特別是,到2022年11月ChatGPT的橫空出現,在社交媒體的渲染下,讓普通公眾也對AI技術有著超越理性的崇拜或恐懼。
現在可以明確的是,AI作為一種工具,可以在多個藥物研發的效率、瓶頸難題上帶來幫助,它仍無法跳脫與顛覆現代藥物研發流程的基礎輪廓。研發藥物的過程依舊異乎尋常地困難,因為在某些關鍵節點,總需要進行反復試錯。
不過,還有一點可以明確的是,若把新藥研發當作是顆抬頭看不見天的碩大蘋果樹,那些已被驗證的經典的藥物靶點就是已被摘完的低垂的果實,現在借助AI技術這把梯子,我們可以嘗試摘取此前已抬頭可見但更高處的果實。但還有一點,仍可能有數量無限的果實隱藏在未能被看見的葉叢之中,即便借助AI也仍需我們撥開遮擋,摸索。
大海撈藥的幫手
現代藥物研發技術的發展歷史大致可分為三個階段:第一個階段可以追溯到19世紀開始,人們能從自然產物中分離出單一的有效成分,依靠藥物化學家的靈感、偶然甚至運氣驅動藥物發現;隨后,由抗生素的發現所引領的20世紀藥物大發現,科學家們開始發現和合成具有藥物效果的新分子結構。20世紀后半葉,基于“靶點”的藥物研發興起,科學家可以選出一個生物機理相對明確的“靶點”,篩選得到可以調節該靶點的化合物,并借助分子模擬、組合化學和自動化高通量篩選、重組DNA技術等新技術進行“理性設計”,藥物發現在20世紀末取得了快速進展。
DAI存款利率已提高至8%:8月7日消息,據MakerDAO旗下借貸協議Spark Protocol頁面顯示,DAI存款利率(DSR)已提高至8%。[2023/8/7 21:28:47]
再到第三個時期,也就是21世紀,隨著基因組學、蛋白質組學的發展,越來越多經過理性設計和優化的生物藥獲批上市,登上歷史舞臺。
想弄清楚AI技術具體在制藥領域能做什么,得先知道現代藥物研發到上市的基礎流程有哪些。一般而言,一款新藥的研發流程包括以下幾個階段:探索階段、藥學研究階段、臨床前生物研究階段、臨床研究階段、以及臨床后的審批上市。
“從早期的靶點發現,到化合物發現,到臨床前至臨床間,甚至審批上市至商業推廣都可以用到AI技術的賦能和加速。”晶泰科技首席科學家張佩宇向界面新聞記者表示,目前而言AI最主要集中應用于化藥及生物藥的發現和臨床前開發階段。
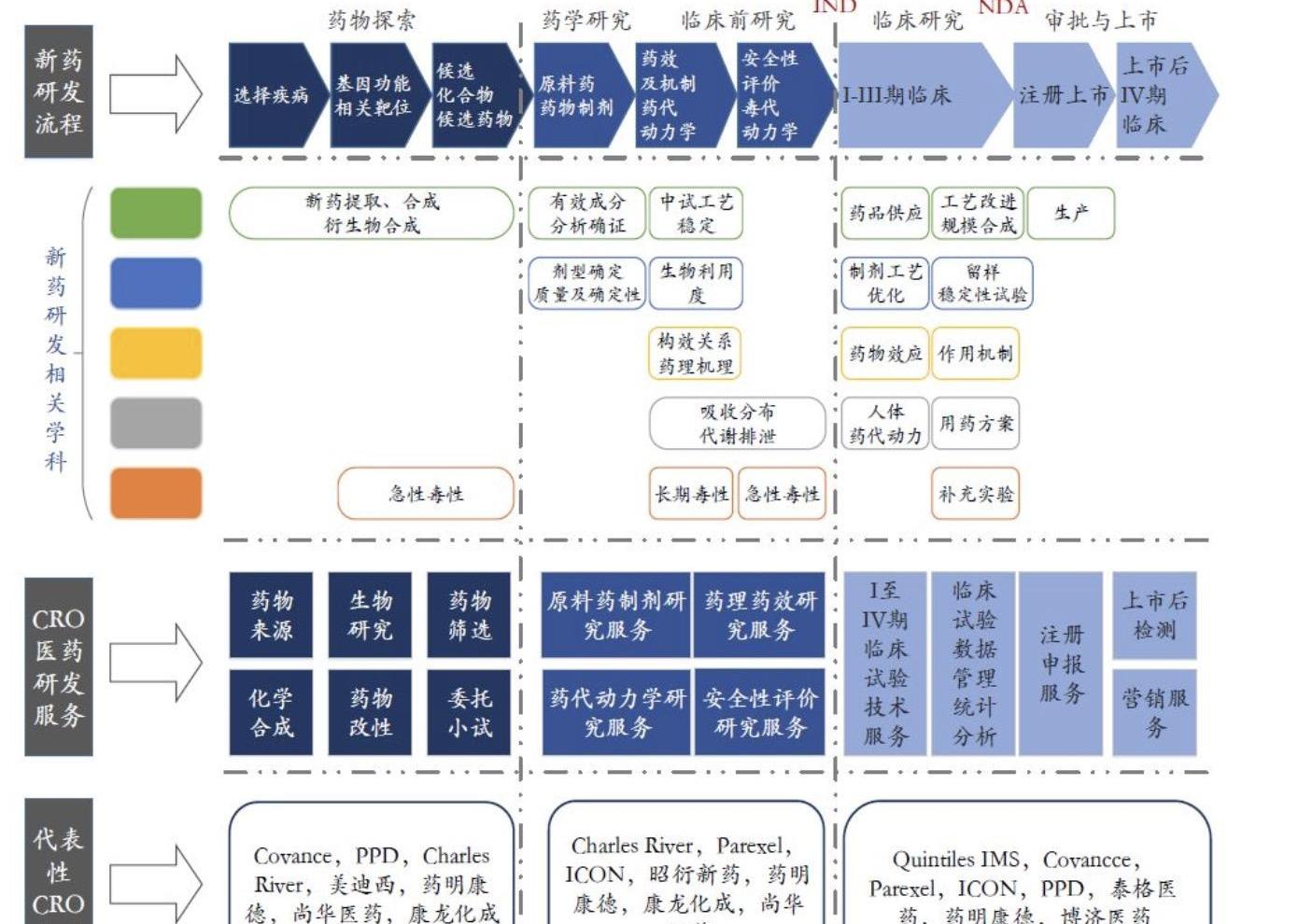
圖片來源:互聯網公開信息
研發一種有效藥物需要兩個條件:一是合適的目標,第二個是合適的化合物。“若把病比作一把鎖,那么靶點就是鎖芯,找到鎖芯,研究出鎖芯的立體結構,那么就可以根據它的立體結構為其設計、打磨一把專有的鑰匙——能夠用藥物治療的藥物即為這把專有的鑰匙。”前賓夕法尼亞大學醫學院研究副教授、杭州賽得康生物科技有限公司創始人張洪濤這樣表示。
而所謂靶點,即人體內能夠與可能成藥的化合物結合,并產生藥理效應的生物大分子的結合部位,現通稱為藥物作用的生物靶點。藥物作用靶點可以是受體、酶、離子通道、轉運體、免疫系統、基因等,其發現和驗證是一個非常復雜的過程。其中,尋找疾病作用機制,發現靶點,是尋找真理的第一步,也是新藥后續能否繼續推進的基石。
以因電影《我不是藥神》而聞名的抗癌藥格列衛為例,它的研發至上市便是依照尋找疾病作用機制,發現靶點這一現代藥物研發流程的基礎輪廓。它也是首款能被稱為是理性設計的藥物——再到基于蛋白質結構篩選和設計能夠抑制靶點蛋白表達的小分子,從生物學原理出發,一步一步都以理性為依據。
在此之前的藥物靶點的發現與應用可以說都是以實驗和經驗觀察主導,有些誤打誤撞的成分。像默沙東90年代研發的治療良性前列腺增生的保列治、和治療男性禿發的保發止。雖然這兩款藥物都是基于5-α還原酶研發的,但默沙東最初的藥物猜測與設計是將其用于抑制青少年粉刺生長。
格列衛是針對慢性粒細胞白血病的靶向治療藥物。罹患慢性粒細胞白血病的患者的血管中的血液里有中性粒細胞。隨著血液里的中性粒細胞越來越多,就會擠占原本血液里紅細胞的資源和空間。紅細胞越來越少后,患者的急癥期便有可能會出現因窒息而死亡的現象。造成這種現象的最底層病理機制便是患者造血干細胞中的基因中的BCR-Abl蛋白出現“故障”——產生中性粒細胞的基因因在中間部分發生交換而無法被正常關閉。這也便是前述所講的患者致病的原因所在,也就是鎖心。
化合物篩選庫包含大量有潛力成為藥物的化合物,通常由以百萬到億計數的小分子組成,既有可購買的商業庫,也有大藥企自己獨有的分子庫,每個化合物都有不同的結構和物理、化學、藥學性質,是藥物發現、篩選和設計的起點。格列衛,其最基礎的、編號為STI571的化合物便是科學家基于成千上萬中小分子中被篩選出的能適配且能打開BCR-Abl蛋白這個鎖心的鑰匙。這在業內也被稱為苗頭化合物,即這些化合物很可能有效。
DefiLlama的ChatGPT插件將進行Beta測試,允許通過語言提示查詢數據:6月4日消息,DefiLlama 創始人 0xngmi 發推表示,DefiLlama 的 ChatGPT 插件將進行 Beta 測試,如果用戶在 ChatGPT 上具有插件訪問權限,并愿意就插件提供反饋,可以加入等待名單。它將允許用戶通過語言提示查詢 DefiLlama 的數據,包括詢問「3 月后哪些 LSD 項目增長最快?」等與數據相關的問題。[2023/6/4 11:56:57]
與此前不同的是,如今,苗頭化合物的發現通過高通量篩選完成。人類合成過的分子是百萬級,一般用于篩選的虛擬化合物庫大到幾十億分子的規模,藥物研發科學家依照計算機輔助技術和個人經驗,選定大概的方向,分批將這些分子按需合成后進行實驗驗證,如果觀察到小分子和靶點的蛋白質有一定的結合能力,再去進一步研究和優化。
在苗頭化合物基礎上,再經過一系列優化和確認后,像進行體內外的活性測試、理評價和藥代動力學研究等,就形成了具有良好的生物活性和較好的藥物性質和安全性的化合物——先導化合物。這一部分也被成為臨床前研究的藥物發現與探索。之后,再經過漫長且風險的臨床試驗、監管審批,某款被驗證的藥物或有最終上市的可能。
實際上,據推算,可能成藥的化合物,也就是鑰匙的個數是10的60次方。這意味著,這比太陽系里的原子數量還要高好幾個數量級。而人類目前所能篩選到的分子數量僅在10的11次方。這中間還存在著巨大的差異。也可以說,前面編號為STI571的化合物能被挑選出來且最終成為知名藥物格列衛也是一個幸運的結果。
目前AI在藥物發現領域的作用,就是在前述的經驗積累中學習為遇到這個幸運再增加一些概率。“如果我們能通過AI打開更大的分子宇宙,或許就有更多格列衛級別的分子能夠橫空出世,攻克新的疾病。”張佩宇表示。
在業內藥物研發的過程被總結為三高一長:高投入、高風險、高回報,但時間長。一款新藥從研發到上市面臨3個“10”的考驗——10年時間、10億美金、10%成功率。像格列衛這樣理性兼顧幸運的產品于2001年5月才終于通過了美國食品藥品管理局審批正式上市,這距離格列衛的所有者諾華向FDA提交藥品上市申請已過去兩年半,而距離找到能打開BCR-Abl蛋白這個鎖心的鑰匙的那一刻已過去十三年。
“在引入AI之前,尋找可能成藥的化合物的篩查過程是人工篩選試驗的,效率低下,進展緩慢,且篩選的先后順序往往是基于研發者個人的經驗,帶有一定的運氣成分,不確定性很高,困難重重。”張佩宇表示,可能能成藥的化合物也要滿足多種屬性。在篩查化合物的過程中,AI能做的如同老頑童的“左右互搏”,AI一邊推測設計出百萬量級的可能成藥的化合物,其中一些可能從未存在于任何藥物數據庫中;一邊就是建立模型,成為這些分子的篩選器,就像巨大的漏斗。在漏斗精挑細下選出最有可能與適配鎖心的化合物,各方面物理化學性質也要滿足可能成藥的標準。“綜合評估被篩選的化合物的成藥性、活性、選擇性,成功概率可能會更大。”
圓壹智慧創始人兼CEO潘麓蓉博士在接受行業媒體同寫意采訪時曾表示,藥物設計有時候需要研究化合物與生物酶的多級作用機制,涉及多口袋競爭、誘導契合、酶催化反應等動態過程。傳統方法或許可以計算單個口袋與化合物結合的物理近似,但處理真實酶催化反應歷程的計算結果與實驗存在很大偏差。而深度學習模型通過“學習”活性實驗數據,將所有“口袋”和“過程”作整體考慮,在訓練充分的情況下,可以產生比傳統物理模擬方法更接近實驗的計算結果。
前FTX工程總監Nishad Singh對美國刑事指控認罪:金色財經報道,據路透社發文稱,前FTX工程總監Nishad Singh對美國刑事指控認罪。此前消息,Alameda首席執行官Caroline Ellison和FTX首席技術官Gary Wang分別承認了七項和四項刑事指控。[2023/3/1 12:34:58]
除了發現可能成藥的化合物的外,AI在小分子藥物自動合成路線的設計、新藥物效果模擬和預測,甚至新型藥物分子的預測上面都有實際應用的實踐。像輝瑞新冠口服藥Paxlovid便是AI在藥物探索階段深度參與和加速的結果。在此之前,行業內的臨床前研究平均需要4-7年時間。
張佩宇介紹,晶泰科技曾幫助輝瑞將研發Paxlovid所需要化合物、及其所有可能的固體形態,通過AI算法全部預測且準確匹配實驗結果。這項工作關乎藥品安全、大規模生產以及專利的申報,原本需要耗時要半年以上,當時通過AI耗費六個星期就已全部預測完成。這為后續的繼續研發大大提前了進程。
“AI既可以有效學習現有分子結構特點,隨機產生大量新的分子結構,也可以按照藥物化學家的需求,定向產生符合某種藥物設計需求的新分子結構,從而大大擴展藥物篩選過程中可用的高質量藥物分子候選者。這種基于海量‘經驗值’的設計能力遠超任何人類科學家。”張佩宇說。
張佩宇表示,藥物研發是多目標優化試錯的過程,也正是如此才需要有借助AI來篩選。傳統試驗人工要合成幾千、上萬個分子,也仍可能失敗。AI就是來提高試錯的成功率。試錯是不可避免的,只不過是借助AI的“比特”而非人手來協助試錯,試錯效率顯著提高,可以將篩選范圍從幾千拓展到百萬,同時顯著降低排除錯誤選項的成本,還能挑戰傳統實驗方法無法勝任的“難成藥靶點”,有望讓藥物走上臨床的成功概率從“萬中無一”變成幾千甚至幾百分之一。
“在藥物研發領域不是單純非黑即白,中間還有非常多的灰度。”張洪濤表示,比如某個制藥企業根據這個有可能成功的靶點做某個蛋白藥物,假設有1千種可能性,就需要雇1千個科研人員去測試它的可能性,但普通的制藥企業根本沒有這么大的資金來實現它,現在通過AI技術將可能的分子提前篩選,原來的1千種可能性縮小集中到最有可能10個,即使不能保證這10個分子最終都能成功,但這聚焦目標的過程就是AI在藥物發現領域目前作出的貢獻。
并非無所不能?
仍需要提醒一句,AI制藥沒法一步到位地實現目標——即脫離前期海量的生物學研究,憑空創造出藥物。像能創造格列衛的STI571這樣有效的化合物,如果沒有真實有效的靶點,若沒有機緣,即便借助AI也有可能不會被找到,就像真理也許并不存在于圖書館之中。
AI的學習資料是基于人類已經創造的實驗數據,對于那些是冷門乃至未知的靶點信息,AI無法準確的無中生有。
如作家納西姆·塔力布在他的暢銷書《黑天鵝》中將未知的未知比喻作“黑天鵝”。在資本市場黑天鵝的出現是令人惶恐不安的,但在新藥研發領域,能夠發現且識別黑天鵝則是令人欣喜若狂——當一個疾病靶點被發現,就可能顛覆一種原本不可能治愈的疾病,催生一系列相關藥物的研發和上市。
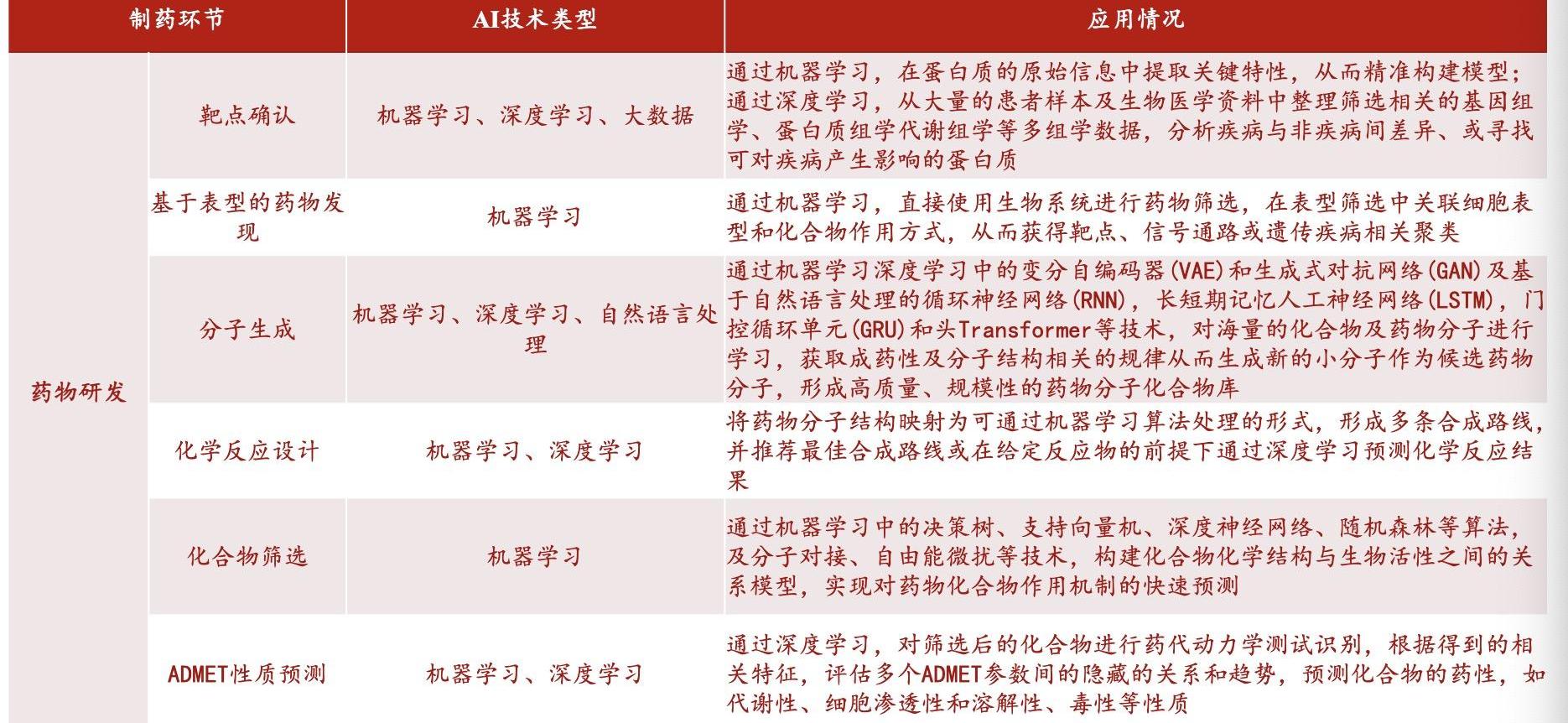
圖片來源:浙商證劵
美國1月未季調CPI年率錄得6.4%,創2021年10月以來最小增幅:金色財經報道,美國1月未季調CPI年率6.4%,預期6.20%,前值6.50%。美國1月未季調核心CPI年率5.6%,預期5.50%,前值5.70%。美國1月未季調CPI年率錄得6.4%,為連續第7個月下降,創2021年10月以來最小增幅。[2023/2/14 12:06:50]
在新藥研發領域,可以將新藥的探索分為兩種:一種是已知的未知,就像默沙東模仿日本第一三共,去尋找幾乎與美伐他汀化學式一摸一樣的洛伐他汀。
對于已知的未知,科學家給AI確定的靶點探索方向通過深度學習模型的介入,可以更快地數以千萬計的科學文獻的非結構數據、以及這些生物的基因分子中找到可能合適的靶點,再通過選擇不同的靶點并進行驗證,以了解靶點的生物學特性,實時交互得到有證據的結果,實現相應藥物靶點的發現。
當然,這種準確性仍不能保證。張佩宇表示,核心競爭力其實是,通過AI推理提出的假設和驗證的時間與人提出的推理假設精確度相比,準確性與效率是否提升。這才是決定人是否在此處使用AI的關鍵。
還有一種是未知的未知,但未知的未知有多少,這連AI也不清楚。
就像前述最初提及的,基于5-α還原酶研發的治療良性前列腺增生的保列治和治療男性禿發的保發止。該理論最初基于早在1948年美國藥理學家雷蒙德·P·安奎斯特就提出的可能——存在兩種不同的腎上腺素受體的假設。
在整整十年后,科學家回溯后才相信,這只黑天鵝早已掠過人類認知的天際,只不過沒有一個人能辨認出它。到了七十五年后的今天,即便有了AI協助,現在的科學家也仍出現與當時相似的情況——可能無法辨認出剛剛劃過天空的就是一只黑天鵝。
“但是通過人對AI的有效利用與兩者的協作,我們或許就具備更好地抓住黑天鵝的機會。”張佩宇說,比如利用AI挖掘潛在的靶點,再基于靶點去篩選潛在的藥物。因為AI制藥的成本更低,甚至可以折疊新靶點驗證和新藥早期發現這兩個順序步驟的時間,通過找到有效的苗頭化合物,反向驗證靶點的真實有效。如同在可能有黑天鵝的位置撒下大網,通過抓住它來驗證它的存在。
此外,即使發現與辨認出了黑天鵝,AI也如前所所言協助著科學家縮小了選擇鑰匙的范圍,但還需對這枚鑰匙進行打磨,之后科學家也還需要再去試驗,再看看是否有效,將數據反饋給AI算法,下一輪生成更加接近需求的鑰匙,從而形成一個循環。這個對鑰匙結合打磨驗證的過程,必須在真實世界完成,需要AI無和實驗技術配合完成。
其中,通過AI虛擬篩選苗頭化合物是藥物開發的一個起點,只是藥物發現過程中的一個步驟,還需要經過多個步驟的篩選和優化。它只能提供初步的篩選結果,需要進一步進行實驗室篩選和結構優化等步驟,才能最終確定苗頭化合物。AI預測良好的活性、穩定性和安全性等方面可能存在一定的不確定性,實驗數據反饋給算法后,可能仍然需要經過若干輪的迭代,和科學家的參與意見,AI才能設計出真正符合要求的分子。
這就像在拼樂高積木,但與標準化的、能完全拼合的樂高積木不同,試驗被挑選的可能能適配打開新靶點這把鎖的化合物過程中,它們間有時候可能會出現只有部分結合的情況,而部分結合又分為大部分結合,或是小部分結合。小到結合位點,大到靶點的微環境,都有其獨特性,很難有“萬金油”算法能夠放之四海而皆準。這樣的結果是,在藥物研發試驗中會有各種千奇百怪的結果。
美國三大股指漲幅擴大,道指漲超1%:金色財經報道,行情顯示,美國三大股指漲幅擴大,道指漲超1%;納指盤中轉漲,此前一度跌超1%。[2022/8/17 12:29:43]
張佩宇表示,每個項目都需要定制化的策略。更重要的是后續的數據反饋閉環,AI在每個靶點體系中經過針對性的數據積累和模型優化。
以前述提及的DeepMind的AlphaFold為例,此前結構生物科學家顏寧回國后,輿論曾熱議其科研成果是否可以被AlphaFold的AI技術直接取代。一位生物醫藥人士曾向界面新聞表示,以AlphaFold2為代表的的AI蛋白結構預測算法,還沒法取代結構生物學的濕實驗。AI技術的確預測來幾乎所有Uniprot中的序列的結構,但這些預測模型的質量仍良莠不齊。
濕實驗指的是在實驗室里采用分子、細胞、生理學試驗方法進行研究,也就是傳統的藥物研發實驗室;而干實驗則是通過計算機模擬及生物信息學方法來進行研究,既有傳統的“計算機輔助藥物設計”,也包括AI藥物研發平臺做的事情。。
另一位生物醫藥人士也曾向界面新聞表示,目前來說AI只能是補充手段,可以減少確定結構過程中的很多麻煩,但最終仍脫離不開科研人員的實驗驗證。“即使你基于當前模型,預測的準確率達100%,也不能在不進行濕實驗的情況下確定該結構的準確性。”
在確認靶點后從苗頭化合物到先導化合物這個試驗階段,先導化合物在體外和體內實驗中已經表現出一定的藥效和選擇性,但在實際應用中,也可能存在潛在的性和不良反應,藥效、生物利用度和代謝等也需要進一步評估和優化。
張洪濤表示,依據AI的學習程度,理論上可以根據已有的數據庫,避免性、不良反應的風險的概率,也仍需要真實的實驗來驗證AI預測的結果是否準確。
不過,就像第一個獲批上市的他汀類藥物,被稱為膽固醇殺手的默沙東歷史上的頭號大藥洛伐他汀。若僅帶著AI技術穿越回去,在沒有數據支持的情況下,即便借助AI也會在當時面臨的抉擇前搖擺不定。
與第一三共于1980年因性而終止研發的美伐他汀相比,默沙東的洛伐他汀在化學結構上“幾乎完全一樣”——唯一的區別就是一個甲基。若用現有的任何一種人工智能算法來做預判,都會認為洛伐他汀也應該會像美伐他汀一樣引起癌癥比例升高的嚴重問題,但默沙東為期兩年的動物性實驗數據卻顯示洛伐他汀沒有出現相同的問題。
張佩宇表示,這的確是目前AI還無法解決的問題。像發現美伐他汀與洛伐他汀的細微差異,這種細微變化相似,但卻導致在人體內的作用效果有巨大差異,面對人體這樣龐大且復雜的體系,目前AI也無法幫助人類走捷徑。這種細微的變化發現就是試錯試出來的,所以臨床試驗仍然是對藥物安全性有效性最權威的考驗。AI協助人類試錯是將錯誤成功率從萬分之一,降到千分之一,再可能降到百分之一,而不是一試一個準。即便只是將臨床試驗成功率從10%提高到20%、30%,也是對創新成功率2、3倍的提升。
而且人體還是一個異常復雜的分子系統,復雜度與尺度遠超現在計算技術的模擬能力,而身體各個組成部分之間的關系極其復雜,牽一發而動全身,且每個個體又有其不同的特性。換句話說,人體的生理活動不像機器人并沒有固定的套路。對于人體內的生理活動,截至目前科學家們只了解其中很小的一部分,仍無法描繪身體中絕大部分分子究竟是如何工作的。這讓藥物的效果在人體試驗的結果依舊無法預測。
張佩宇表示,人類的探索和嘗試從未停止。目前的藥物研發在細胞、酶等試管環境探究其初步的有效性,再在由小到大的動物模型中進一步探索藥物在生物體內的藥效,直至走上臨床。而類器官等技術與AI的結合,可以在試管中更好地復原和模擬人體內的三維環境,讓藥物研發早期獲得與真實臨床相關性更高的活性數據,這樣訓練出來的AI模型,有望設計和篩選出臨床成功率更高的藥物分子。
未來的野望
在1950年發表的作品《我,機器人》中,歷史上最偉大的科幻小說作者阿西莫夫深入探討了“機器人學三定律”:
第一法則:機器人不得傷害人類,或袖手旁觀坐視人類受到傷害;第二法則:除非違背第一法則,機器人必須服從人類的命令;第三法則:在不違背第一及第二法則下,機器人必須保護自己。
以人類現在的局限性,無法透支未來的圖景,但有一點可以明確:現在的在AI被用于新藥研發的環節仍需人類制定或給予方向。
“人類很容易把想法收斂到某個方向再去推理闡釋,這是人的優勢。”張佩宇表示,現階段AI的確可以根據人設定的目標去自發探索,但人給予明確的方向AI探索的效率會更高。
若明確AI作為工具,至少在新藥研發領域,現在很多關于AI的崇拜或恐懼或可以煙消云散。
“人和AI結合起來做藥物探索與發現是未來新藥研發行業的事實趨勢。不會使用AI的科學家會被會使用AI的科學家取代,并不是說AI會完全取代科學家。”張佩宇說。
生物醫藥將是AI產業化最重要的部分之一。傳統的制藥模式中,藥物從頭設計依賴于專家經驗指導下的實驗試錯,且新藥篩選失敗率高、藥企的創新投資回報率不斷下降。如何通過大數據、人工智能等科學技術,更加高效地以“比特“而非實驗去試錯,從而加速新藥研發進程、平衡研發投入與成果產出之間的關系,成為了醫藥公司在數字化改革道路上的重點之一。
據浙商證劵數據,2022年醫藥行業的投融資熱度下降,但AI制藥賽道反而更加火熱。根據公開數據統計,2022年全年AI制藥賽道相關的融資總事件達144起,YOY97%,總金額為62.02億美元,YOY47.67%。且美國AI初創公司吸納了市場上的絕大部分資金,占總融資額的77%。
界面新聞了解,前AI制藥市場的主要參與者有三類:生物醫藥企業、CRO、互聯網公司。在商業模式上主要分為:AI-biotech、AI-CRO和AI-SaaS,即利用AI自己建立新藥研發管線成為藥企、提供藥物發現服務和售賣AI藥研平臺與軟件的使用服務。
像互聯網公司借助對外投資、打造自有相關平臺、提供算力及計算框架服務,但像騰訊、百度、字節跳動等互聯網公司的缺點在于,他們雖然算法和算力優勢,但對制藥專業領域的知識及經驗較為匱乏,而現階段的AI制藥在模型與數據之外,仍需要大量物理、化學、生物學、藥學等領域算法與方法的跨界融合,是需要到多目標優化的系統工程。因此互聯網公司主要集中發力在新藥研發對數據及算力要求較高的環節,有同質化競爭趨向,到了CMC之后的階段算法和算力提供的幫助就變得有限,也很難拿到顯著優越于同行的結果,說服藥企為平臺的落地付費買單。
除去售賣軟件外,AI+CRO和AI+Biotech是目前被資本市場認可的最主流的商業模式。實際上,資本市場對是做AI+CRO還是AI+Biotech之間仍有分歧。不過,在分歧中也走出了各種的頭部。其中,晶泰科技更偏AI+CRO,而英矽智能則更偏AI+Biotech。
當然,這兩種不同的商業模式也會帶來不同的風險與回報。AI+Biotech則可能采取構建伙伴關系或內部藥物發現為商業模式。這兩種的AI制藥商業模式的底層邏輯與Biotech無異。
選擇AI+Biotech模式的公司最主要原因是依照生物醫藥行業慣性:一個成功的藥物一旦進入市場,每年很大概率能給公司帶來數億乃至數十億美元的回報,直到專利過期。他們在內部開發候選藥物,通過臨床試驗的考核,最終將產品推向市場。在藥物正式批準上市之前,按照市場慣例,公司估值與管線的表現高度關聯,隨著藥物管線進入I、II、III期臨床,公司估值也會水漲船高;而某次臨床失利的消息也可能直接讓企業估值受創。但仍要提醒的是,藥物發展路徑仍漫長且充滿風險,臨床研究需要數年時間且花費昂貴,即便借助AI也不例外。
諸如英矽智能、未知君、藥物牧場等早期的AI制藥公司在定位上便是明顯的Biotech特征。這些公司均有多個在研管線,并且擁有已進入臨床階段的管線,目標是打造First-in-class或best-in-class藥物,推動這些藥物管線上市或被大藥企接盤。
選擇AI+CRO模式的公司,會將其AI研發技術與服務作為產品出售給制藥和生物技術公司。他們與合作伙伴合作,完成特定的研發環節,或包圓整個靶點發現后到臨床前驗證的環節,然后將臨床候選移交給合作伙伴繼續進行新藥申報的準備和臨床開發與研究。這種商業模式使選擇AI+CRO模式的公司能夠專注在AI最有優勢的、輕資產投入而重計算的臨床前環節,最大限度地優化、提高其平臺的效率,甚至實現新藥研發的規模化效應,最主要的是能避免新藥研發更下游開發的風險,同時可以收到新藥一步步走向上市的里程碑付款甚至分享銷售分成。
像晶泰科技與禮來簽署一項AI小分子新藥發現合作,預付款及里程碑總收益可達2.5億美元,也是目前國內最大的單個管線AI新藥發現合作訂單。
“現在AI制藥企業技術布局趨向同質化,AI制藥企業應該打造自己獨特的技術優勢,根據不同的新藥研發需求提供相適配的服務”,張佩宇表示,晶泰科技不會做Biotech模式,因為Biotech實際上能做的項目很少。晶泰科技也不會是純粹的CRO模式,傳統的CRO模式是按勞動力付費的,多一倍的項目就需要招多一倍的人。而AI+CRO是可以實現藥物研發規模化,研發的管線越多,數據的積累與算法的優化優勢越明顯,平臺的交付能力越強,且邊際效應明顯——因為預測可以減少高達90%的傳統實驗需求,所以在大量云計算資源的支持下,服務的管線數量翻倍,也不需要等比翻倍地招募更多的人來為項目服務。
關于AI制藥的未來構想無論多么宏大,對于所有的AI制藥企業來說,有個必須探討的阿喀琉斯之踵——數據如何得來?張佩宇也直言,AI的核心三要素,算力、算法、數據,如果大家都相差不多,也很難有企業殺出重圍,在同質化競爭中異軍突起。在算法模型快速發展、云端算力極大豐富的今天,數據成了發展AI制藥最關鍵的瓶頸。
但醫藥行業目前所擁有的數據規模和質量,在一些研發環節的數據是不足或者數據構成單一、一致性差,直接影響模型表現。與ChatGPT直接搜羅學習全互聯網的公開信息不同,AI在制藥方面的數據積累就困難的多,比如一個分子是否對給定的靶點有活性,需要在將這個分子真正合成出來,再經過一系列的實驗測試。這期間的耗費的時間周期與數據獲取和標注成本要高很多。
特別是,制藥領域涉及專利,對數據開源和分享的意愿很低,且非常注重數據安全與隱私保護。擁有獨特、豐富的化合物數據集是成功制藥公司的法寶,有些更是通過多年專注于某一個疾病靶點或生物學領域,積累了大量獨家的實驗數據,這對藥企來說是關鍵的數字化資產和研發優勢。而對數據極度依賴的、需要高度開放的AI要想在藥物研發領域落地,并促成質的提升。
張佩宇表示,現在的核心是需要解決什么問題就搜集什么數據。與藥企合作也會在藥企的要求下使用相關的數據庫,包括通過隱私計算,針對藥企數據去訓練模型,但這些數據的所有權依舊歸于藥企所有。但AI可以通過不斷的學習完善自己的模型。
“目前行業普遍認為,AI需要與濕實驗相輔相成,“干濕結合”才是對AI技術最好的使用。”張佩宇表示,自動化與AI的結合使用也是行業未來的趨勢。自動化實驗能夠收集大量的數據,還有望解決AI藥物研發的數據短板問題,有助于提升整體研發流程的效率和成功率。大量重復性勞動交給機器人,科學家將有更多時間和精力投入到藥物研發的關鍵環節中,不僅實驗產出效率成倍提升,還能減少人為操作引起的實驗誤差。
前有比亞迪高管預測高考作文題,后有日本出版社高調拆解比亞迪海豹,還制成書出版,售價高達4.5萬,最近比亞迪一直在熱搜上下不來啊.
1900/1/1 0:00:00新聞標題定位提示: 億歐網創始人黃淵普舉報知乎創始人周源→公司新聞排行榜NO.6內蒙古新井煤礦坍塌事故搜救結束.
1900/1/1 0:00:00如果說起今天的北京,一定會有很多人脫口而出“鳥巢”兩個字。2008年奧運會之后,鳥巢已經成了北京的標志性建筑。作為“二十一世紀初葉最有特點的建筑”,鳥巢成為很多人心中無法替代的存在.
1900/1/1 0:00:00一、項目簡介和融資信息 近年來,人工智能技術的發展一直在各個領域引起了轟動。然而,OpenAI創始人Sam并不僅僅滿足于已有的成就,他正在策劃下一個顛覆性的項目——加密貨幣領域的“WorldCo.
1900/1/1 0:00:00公司 6月18日,億緯鋰能宣布成立醫療電池事業部。億緯鋰能表示,未來將建立醫療電池標準。6月16日晚間,極兔速遞在港交所提交上市申請,擬募資5億-10億美元.
1900/1/1 0:00:00虛擬貨幣是指基于互聯網和加密技術,使用數字代碼作為價值儲存和交換媒介的一種貨幣形式。虛擬貨幣不像傳統貨幣一樣有實體形態,而是以電子數據形式存在于互聯網上.
1900/1/1 0:00:00